Integrantes:
Erick Joaquin Ortiz Madrid
Alondra Gonzales de la Cruz
Jennifer Sosa Perez
Diana Laura Escobar Martinez
2H
esc. cetis 61
Norma Sierra
Quimica 2
LOS MOLES
jueves, 31 de mayo de 2012
miércoles, 30 de mayo de 2012
El carbono es un elemento químico de número atómico 6 y símbolo C. Es sólido a temperatura ambiente. Dependiendo de las condiciones de formación, puede encontrarse en la naturaleza en distintas formas alotrópicas, carbono amorfo y cristalino en forma de grafito o diamante. Es el pilar básico de la química orgánica;
se conocen cerca de 16 millones de compuestos de carbono, aumentando
este número en unos 500.000 compuestos por año, y forma parte de todos
los seres vivos conocidos. Forma el 0,2 % de la corteza te
rrestre.
la isomeria
La isomería
La isomería es una propiedad de ciertos compuestos químicos que con igual fórmula molecular (fórmula química no desarrollada) es decir, iguales proporciones relativas de los átomos que conforman su molécula, presentan estructuras moleculares distintas y, por ello, diferentes propiedades. Dichos compuestos reciben la denominación de isómeros. Los isómeros son compuestos que tienen la misma fórmula molecular pero diferente fórmula estructural y, por tanto, diferentes propiedades. Por ejemplo, el alcohol etílico o etanol y el éter dimetílico son isómeros cuya fórmula molecular es C2H6O.
Aunque este fenómeno es muy frecuente en Química orgánica, no es exclusiva de ésta pues también la presentan algunos compuestos inorgánicos, como los compuestos de los metales de transición.

La isomería es una propiedad de ciertos compuestos químicos que con igual fórmula molecular (fórmula química no desarrollada) es decir, iguales proporciones relativas de los átomos que conforman su molécula, presentan estructuras moleculares distintas y, por ello, diferentes propiedades. Dichos compuestos reciben la denominación de isómeros. Los isómeros son compuestos que tienen la misma fórmula molecular pero diferente fórmula estructural y, por tanto, diferentes propiedades. Por ejemplo, el alcohol etílico o etanol y el éter dimetílico son isómeros cuya fórmula molecular es C2H6O.
Clasificación de los isómeros en Química orgánica.
Tipos de isomeros:
Isomería de cadena o esqueleto.- Los isómeros de este tipo tienen componentes de la cadena acomodados en diferentes lugares, es decir las cadenas carbonadas son diferentes, presentan distinto esqueleto o estructura.
Isomería de posición.- Es la de aquellos compuestos en
los que sus grupos funcionales o sus grupos sustituyentes están unidos
en diferentes posiciones.
Un ejemplo simple de este tipo de isomería es la del pentanol, donde existen tres isómeros de posición: pentan-1-ol, pentan-2-ol y pentan-3-ol.
Isomería de grupo funcional.- Aquí, la diferente
conectividad de los átomos, puede generar diferentes grupos funcionales
en la cadena. Un ejemplo es el ciclohexano y el 1-hexeno, que tienen la
misma fórmula molecular (C6H12), pero el ciclohexano es un alcano
cíclico o cicloalcano y el 1-hexeno es un alqueno. Hay varios ejemplos
de isomeria como la de ionización, coordinación, enlace, geometría y
óptica.
Isomería de cadena u ordenación
Varía la disposición de los átomos de C en la cadena o esqueleto
carbonado, es decir la estructura de éste, que puede ser lineal o tener
distintas ramificaciones.
 |
 |
|---|
Para la fórmula C5H12, tenemos tres posibles isómeros de cadena: pentano, metilbutano (isopentano) y dimetilpropano (neopentano). El número de isómeros de cadena crece rápidamente al aumentar el número de átomos de carbono.
Isomería de posición
La presentan aquellos compuestos que poseen el mismo esqueleto carbonado pero en los que el grupo funcional o el sustituyente ocupa diferente posición.
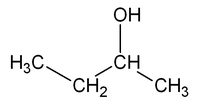
Por ejemplo, la fómula molecular C4H10O puede corresponder a dos sustancias isómeras que se diferencian en la posición del grupo OH: el 1-butanol y el 2-butanol.
| CH3-CH2-CH2-CH2OH | CH3-CH2-CHOH-CH3 |
|---|---|
| 1-butanol, Butan-1-ol o n-butanol | 2-butanol, Butan-2-ol o sec-butanol |
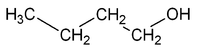 |
 |
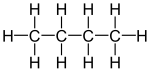
Este tipo de isomería resulta de la posibilidad de colocar grupos funcionales, cadenas laterales o átomos sustituyentes en posiciones estructuralmente no equivalentes. Supongamos que sustituimos uno de los átomos de hidrógeno del butano, CH3-CH2-CH2-CH3, por un grupo hidroxilo.
Numerando los carbonos de la cadena del butano y realizando esta
sustitución en el carbono extremo (C1), obtenemos un alcohol llamado
butan-1-ol (1-butanol). Si sustituimos un hidrógeno del C2 por el grupo -OH, obtenemos el alcohol isómero butan-2-ol (2-butanol),
que difiere en la posición del grupo hidroxilo. Obsérvese que, sin
embargo, si realizamos la sustitución en el C3, no obtenemos un tercer
isómero, sino de nuevo el 2-butanol. Las dos representaciones que se
indican para el 2-butanol son estructuralmente idénticas, como se puede
ver girando su estructura 180º alrededor de un eje.
Isomería de compensación o por compensación
A veces se llama isomería de compensación o metamería la de aquellos compuestos en los cuales una función corta la cadena carbonada en porciones de longitudes diferentes.
Por ejemplo tres metámeros de fórmula molecular C402H8 son:
| HCOO-CH2-CH2-CH3 | CH3-COO-CH2-CH3 | CH3-CH2-COO-CH3 |
|---|---|---|
| Metanoato de propilo | Etanoato de etilo | Propanoato de metilo |
Este tipo de isomería era más usado en el pasado que en la actualidad. Se aplicaba incluso a aldehídos-cetonas, a los que hoy se suelen considerar isómeros de función.
Isomería de función
Varía el grupo funcional, conservando el esqueleto carbonado.
Por ejemplo el C3H6O puede corresponder a la molécula de propanal (función aldehído) o a la Propanona (función cetona).
| CH3-CH2-CH0 | CH3-CO-CH3. |
|---|---|
| Propanal (función aldehído) | Propanona (función cetona) |
Esta isomería la presentan ciertos grupos de compuestos relacionados como: los alcoholes y éteres, los ácidos y ésteres, y también los aldehídos y cetonas.
Isomería espacial o estereoisomería
Presentan estereoisomería aquellos compuestos que tienen fórmulas
moleculares idénticas y sus átomos presentan la misma distribución (la
misma forma de la cadena; los mismos grupos funcionales y sustituyentes;
situados en la misma posición), pero su disposición en el espacio es
distinta, o sea, difieren en la orientación espacial de sus átomos.
Los isómeros tienen igual forma en el plano. Es necesario
representarlos en el espacio para visualizar las diferencias. Puede ser
de dos tipos: isomería conformacional e isomería configuracional, según que los isómeros se puedan convertir uno en otro por simple rotación de enlaces simples, o no.
Otra clasificación los divide en enantiómeros (son imágenes especulares) y diastereoisómeros
(no son imágenes especulares). Entre los diastereoisómeros se
encuentran los isómeros cis-trans (antes conocido como isómeros
geométricos), los confórmeros o isómeros conformacionales y, en las
moléculas con varios centros quirales, los isómeros que pertenecen a
distintas parejas de enantiómeros.
Isomería conformacional
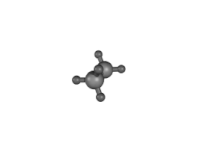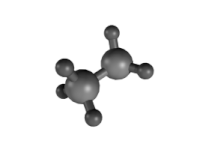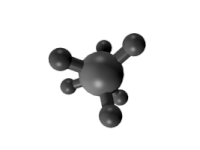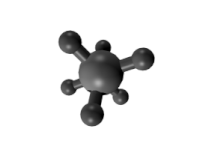
En este tipo de isómeros conformacionales o confórmeros, la conversión de una forma en otra es posible pues la rotación
en torno al eje del enlace formado por los átomos de carbono es más o
menos libre (ver animación a la derecha). Por eso también reciben el
nombre de rotámeros. Si los grupos son voluminosos podría haber impedimento estérico y no ser tan fácil la interconversión entre rotámeros.
Los isómeros conformacionales generalmente no son separables o
aislables, debido a la facilidad de interconversión aun a temperaturas
relativamente bajas. La rama de la estereoquímica que estudia los
isómeros conformacionales que sí son aislables (la mayoría son derivados
del bifenilo) se llama atropisomería.
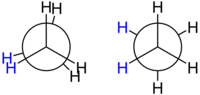
Estas formas se reconocen bien si utilizamos la proyección de Newman,
como se aprecia en los dibujos de la izquierda. Reciben nombres como
sinclinal (a veces, gauche), anticlinal (anti o trans), sinperiplanar y
antiperiplanar.
| Proyecciones de Newmann para la molécula de etano. Formas eclipsada y alternada. | Distintas conformaciones del etano según la rotación en torno al eje que forman los dos átomos de carbono. Se observan formas eclipsadas o formas escalonadas. |
Otro tipo de isómeros conformacionales se da en compuestos con ciclos hexagonales,como el ciclohexano, donde son factibles la conformación en forma de silla y conformación en forma de bote.
Isomería configuracional
No basta una simple rotación para convertir una forma en otra y
aunque la disposición espacial es la misma,los isómeros no son
interconvertibles. Se divide en: isomería geométrica o cis-trans, e isomería óptica.
Los isómeros configuracionales son aislables, ya que es necesaria una
gran cantidad de energía para interconvertirlos (se requiere energía
necesaria para la ruptura de enlaces),
Isomería geométrica o cis-trans
Artículo principal: Isomería cis-trans.
Se produce cuando hay dos carbonos unidos con doble enlace que tienen
las otras valencias con los mismos sustituyentes (2 pares) o con dos
iguales y uno distinto.
No se presenta isomería geométrica ligada a los enlaces triples o sencillos.
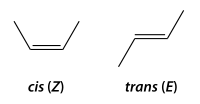
A las dos posibilidades se las denomina:
- forma cis (o forma Z), con los dos sustituyentes más voluminosos del mismo lado, y
- forma trans (o forma E), con los dos sustituyentes más voluminosos en posiciones opuestas.
No se pueden interconvertir entre sí estas dos formas de un modo
espontáneo, pues el doble enlace impide la rotación, aunque sí pueden
convertirse a veces, en reacciones catalizadas.
| Isómeros del But-2-eno | Ácido maleico (Cis) y ácido fumárico (trans) |
Formas trans (E) y cis (Z) del 1,2-dibromoeteno. |
|---|---|---|
 |
 |
La isomería geométrica también se presenta en compuestos con doble
enlace N=N, o en compuestos cíclicos en los que también se impide la
rotación en torno a un eje.
| 1,2-dimetilciclopentano (formas cis y trans) |
cis-1,2-diclorociclohexano | trans-1,2-diclorociclohexano | Formas cis y trans del difluorodiazeno |
|---|---|---|---|
 |
 |
 |
 |
Isomería óptica o Enantiomería
Cuando un compuesto tiene al menos un átomo de Carbono asimétrico o quiral, es decir, un átomo de carbono con cuatro sustituyentes diferentes, pueden formarse dos variedades distintas llamadas estereoisómeros ópticos, enantiómeros, formas enantiomórficas o formas quirales, aunque todos los átomos están en la misma posición y enlazados de igual manera. Esto se conoce como regla de Level y Van't Hoff.
Los isómeros ópticos no se pueden superponer y uno es como la imagen
especular del otro, como ocurre con las manos derecha e izquierda.
Presentan las mismas propiedades físicas y químicas pero se diferencian
en que desvían el plano de la luz polarizada en diferente dirección:
- un isómero desvía la luz polarizada hacia la derecha (en orientación con las manecillas del reloj) y se representa con el signo (+): es el isómero dextrógiro o forma dextro;
- el otro isómero óptico la desvía hacia la izquierda (en orientación contraria con las manecillas del reloj) y se representa con el signo (-)(isómero levógiro o forma levo).
Otra forma de nombrar estos compuestos es mediante el convenio o nomenclatura D-L, normalmente empleando la proyección de Fischer. Esta nomenclatura es absoluta pero no necesariamente la forma (D) coincide con el isómero dextrógiro o forma (+).
Si una molécula tiene n átomos de Carbono asimétricos, tendrá un total de 2n isómeros ópticos.
También pueden representarse estos isómeros con las letras (R) y (S). Esta nomenclatura R-S, que sigue las reglas de Cahn-Ingold-Prelog, también se utiliza para determinar la configuración absoluta de los carbonos quirales.
Así pues, hay tres sistemas de nombrar estos compuestos:
- según la dirección de desviación del plano de la luz polarizada, distinguimos las formas dextro (+) y levo (-);
- según la nomenclatura D-L (Formas D y L), que es inequívoca para isómeros con un solo carbono asimétrico, y
- según la configuración absoluta R-S (formas R y S), más adecuada para moléculas con varios centros asimétricos.
Diasteroisómeros
Artículo principal: Diastereoisómero.
Cuando un compuesto tiene más de un carbono asimétrico podemos
encontrar formas enatiómeras (que son imagen especular una de la otra) y
otras formas que no son exactamente copias espaculares, por no tener
todos sus carbonos invertidos. A estas formas se les llama diasteroisómeros.
Por ejemplo, el 3-bromo-butan-2-ol posee dos carbonos asimétricos por
lo que tiene 4 formas posibles. De ellas, algunas son enantiomorfas
(formas especulares), como (2S,3S)-3-bromo-butan-2-ol y
(2R,3R)-3-bromo-butan-2-ol. En cambio, (2R,3S)-3-bromo-butan-2-ol es un
diastereoisómero de los dos anteriores.
Mezcla racémica y formas meso
Una mezcla racémica
es la mezcla equimolecular de los isómeros dextro y levo. Esta fórmula
es ópticamente inactiva (no desvía el plano de la luz polarizada). La
mezcla de ácido D-láctico y L-láctico forma una mezcla racémica,
ópticamente inactiva..
Si un compuesto posee dos carbonos asimétricos, puede tener uno
dextrógiro y otro levógiro, pero si tiene un plano de simetría, en
conjunto se comporta como ópticamente inactivo y recibe el nombre de forma meso. Es el caso del ácido tartárico o 2,3-dihidroxibutanodioico, uno de cuyos isómeros es una forma meso.
Poder rotatorio específico Es la desviación que sufre el plano de polarización al atravesar la luz polarizada una disolución con una concentración de 1 gramo de sustancia por cm³ en un recipiente de 1 dm de altura. Es el mismo para ambos enantiómeros, aunque de signo contrario. Se mide con el polarímetro.
Isomería en Química Inorgánica
Hay varios tipos de isomeria presente en compuestos inorgánicos, sobre todo en complejos de coordinación, pero este fenómeno no es tan importante como en química orgánica:
- Isomería estructural o topológica: Los átomos se unen de modo diferente, como en el S2F2, de los que existe una molécula en forma de cadena y otra en forma de pirámide triangular. Un caso especial es la tautomería, en la que un átomo de H cambia de posición.
- Isomería conformacional: Igual a la ya comentada para compuestos orgánicos. Se presenta en compuestos con enlace sencillo como P2H4 o el ion ditionito, S2O42-, donde existen formas eclipsadas, escalonadas y sinclinal (gauche).
- Isomería cis-trans (geométrica): Aparece en compuestos como el ácido nitroso, HNO2, o en complejos de coordinación plano-cuadrados como [PtCl2(NH3)2].
- Isomería de posición, como en algunos heterociclos de azufre y nitrógeno. En el S6(NH)2 se mantiene el anillo octogonal del azufre pero dos átomos de azufre han sido sustituidos por grupos NH,que pueden estar en posición 1,2; 1,3; 1,4 y 1,5.
- Isomería óptica: también aparece en compuestos de coordinación de estructura tetraédrica con sustituyentes diferentes.
- Isomería de ionización: Se intercambian un ligando del catión con uno delos aniones que loneutralizan,como ocurre entre [CrSO4(NH3)5]Cl y [CrCl(NH3)5]SO4
- Isomería de coordinación: Si ambos iones son complejos, podemos intercambiar sus ligandos y obtendremos isómeros diferentes, como ocurre entre [Co(NH3)6][Cr(CN)6] [Cr(NH3)6][Co(CN)6].
- Isomería de enlace: Algunos ligandos pueden unirse de modo diferente al ion central,como ocurre en [CoCl(NO2)(NH3)4]+ [CoCl(ONO)(NH3)4]
- Isomería de polimerización: Es el caso de NO2 y N2O4, dos óxidos de nitrógeno gaseosos.
Suscribirse a:
Entradas (Atom)